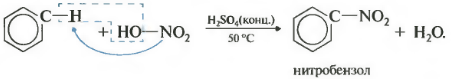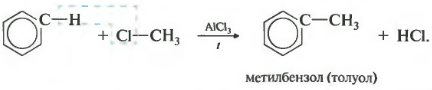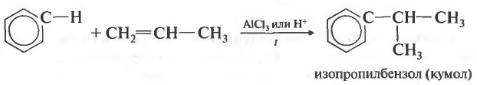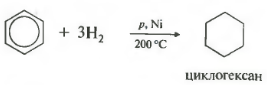Реакция замещения происходит при взаимодействии бензола с. Химические свойства бензола и его гомологов
ОПРЕДЕЛЕНИЕ
Бензол - это бесцветная жидкость с характерным запахом; температура кипения 80,1 o С, температура плавления 5,5 o С. Не растворим в воде, токсичен.
Ароматические свойства бензола, определяемые особенностями его структуры, выражаются в относительной устойчивости бензольного ядра, несмотря на непредельность бензола по составу. Так, в отличие от непредельных соединений с этиленовыми двойными связями, бензол устойчив к действию окислителей.
Рис. 1. Строение молекулы бензола по Кекуле.
Получение бензола
К основным способам получения бензола относятся:
— дегидроциклизация гексана (катализаторы - Pt, Cr 3 O 2)
CH 3 -(CH 2) 4 -CH 3 → C 6 H 6 + 4H 2 (t o C, p, kat = Cr 2 O 3);
— дегидрированиециклогексана
C 6 H 12 → C 6 H 6 + 3H 2 (t o C, kat = Pt, Ni);
— тримеризация ацетилена (реакция протекает при нагревании до 600 o С, катализатор - активированный уголь)
3HC≡CH → C 6 H 6 (t = 600 o C, kat = С activ).
Химические свойства бензола
Для бензола характерны реакции замещения, протекающие по электрофильному механизму:
Галогенирование (бензол взаимодействует с хлором и бромом в присутствии катализаторов - безводных AlCl 3 , FeCl 3 , AlBr 3)
C 6 H 6 + Cl 2 = C 6 H 5 -Cl + HCl;
— нитрование (бензол легко реагирует с нитрующей смесью - смесь концентрированных азотной и серной кислот)

— алкилирование алкенами
C 6 H 6 + CH 2 =CH-CH 3 → C 6 H 5 -CH(CH 3) 2
Реакции присоединения к бензолу приводят к разрушению ароматической системы и протекают только в жестких условиях:
— гидрирование (продукт реакции — циклогексан)
C 6 H 6 + 3H 2 → С 6 H 12 (t o C, kat = Pt);
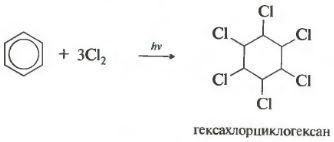
— присоединение хлора (протекает под действием УФ-излучения с образованием твердого продукта - гексахлорциклогексана (гексахлорана) - C 6 H 6 Cl 6)
C 6 H 6 + 6Cl 2 →C 6 H 6 Cl 6 .
Применение бензола
Бензол широко используется в промышленной органической химии. Практически все соединения, имеющие в своем составе бензольные кольца, получаются из бензола, например, стирол, фенол, анилин, галогензамещенные арены. Бензол используется для синтеза красителей, поверхностно-активных веществ, фармацевтических препаратов.
Примеры решения задач
ПРИМЕР 1
| Задание | Плотность паров вещества 3,482г/л. Его пиролиз дал 6 г сажи и 5,6 л водорода. Определите формулу этого вещества. |
| Решение | Сажа представляет собой углерод. Найдем количество вещества сажи исходя из условий задачи (молярная масса углерода равна 12 г/моль):
n(C) = m(C) / M(C); n(C) = 6 / 12 = 0,5 моль. Рассчитаем количество вещества водорода: n(H 2) = V(H 2) / V m ; n(H 2) = 5,6 / 22,4 = 0,25 моль. Значит, количество вещества одного атома водорода будет равно: n(H) = 2 × 0,25 = 0,5 моль. Обозначим количество атомов углерода в молекуле углеводорода за «х», а количество атомов водорода за «у», тогда соотношение этих атомов в молекуле: х: у = 0,5: 0,5 =1:1. Тогда простейшая формула углеводорода будет выражаться составом СН. Молекулярная масса молекулы состава СН равна: М(СН) = 13 г/моль Найдем молекулярную массу углеводорода исходя из условий задачи: M (C x H y) = ρ×V m ; M (C x H y) = 3,482×22,4 = 78 г/моль. Определим истинную формулу углеводорода: k= M(C x H y)/ М(СН)= 78/13 =6, следовательно, коэффициенты «х» и «у» нужно умножить на 6 и тогда формула углеводорода примет вид C 6 H 6 . Это бензол. |
| Ответ | Искомый углеводород имеет состав C 6 H 6 . Это бензол. |
ПРИМЕР 2
| Задание | Рассчитайте количество вещества ацетилена, которое понадобится для получения 400 мл бензола (плотность 0,8 г/мл). | ||||||||||
| Решение | Запишем уравнение реакции получения бензола из ацетилена:
ОПРЕДЕЛЕНИЕ Бензол (циклогексатриен – 1,3,5) – органическое вещество, простейший представитель ряда ароматических углеводородов. Формула – С 6 Н 6 (структурная формула – рис. 1). Молекулярная масса – 78, 11. Рис. 1. Структурные и пространственная формулы бензола. Все шесть атомов углерода в молекуле бензола находятся в sp 2 гибридном состоянии. Каждый атом углерода образует 3σ-связи с двумя другими атомами углерода и одним атомом водорода, лежащие в одной плоскости. Шесть атомов углерода образуют правильный шестиугольник (σ-скелет молекулы бензола). Каждый атом углерода имеет одну негибридизованную р-орбиталь, на которой находится один электрон. Шесть р-электронов образуют единое π-электронное облако (ароматическую систему), которое изображают кружочком внутри шестичленного цикла. Углеводородный радикал, полученный от бензола носит название C 6 H 5 – — фенил (Ph-). Химические свойства бензолаДля бензола характерны реакции замещения, протекающие по электрофильному механизму: — галогенирование (бензол взаимодействует с хлором и бромом в присутствии катализаторов – безводных AlCl 3 , FeCl 3 , AlBr 3) C 6 H 6 + Cl 2 = C 6 H 5 -Cl + HCl; — нитрование (бензол легко реагирует с нитрующей смесью – смесь концентрированных азотной и серной кислот) — алкилирование алкенами C 6 H 6 + CH 2 = CH-CH 3 → C 6 H 5 -CH(CH 3) 2 ; Реакции присоединения к бензолу приводят к разрушению ароматической системы и протекают только в жестких условиях: — гидрирование (реакция протекает при нагревании, катализатор – Pt) — присоединение хлора (протекает под действием УФ-излучения с образованием твердого продукта – гексахлорциклогексана (гексахлорана) – C 6 H 6 Cl 6) Как и любое органическое соединение бензол вступает в реакцию горения с образованием в качестве продуктов реакции углекислого газа и воды (горит коптящим пламенем): 2C 6 H 6 +15O 2 → 12CO 2 + 6H 2 O. Физические свойства бензолаБензол – жидкость без цвета, но обладающая специфическим резким запахом. Образует с водой азеотропную смесь, хорошо смешивается с эфирами, бензином и различными органическими растворителями. Температура кипения – 80,1С, плавления – 5,5С. Токсичен, канцероген (т.е. способствует развитию онкологических заболеваний). Получение и применение бензолаОсновные способы получения бензола: — дегидроциклизация гексана (катализаторы – Pt, Cr 3 O 2) CH 3 –(CH 2) 4 -CH 3 → С 6 Н 6 + 4H 2 ; — дегидрирование циклогексана (реакция протекает при нагревании, катализатор – Pt) С 6 Н 12 → С 6 Н 6 + 4H 2 ; — тримеризация ацетилена (реакция протекает при нагревании до 600С, катализатор – активированный уголь) 3HC≡CH → C 6 H 6 . Бензол служит сырьем для производства гомологов (этилбензола, кумола), циклогексана, нитробензола, хлорбензола и др. веществ. Ранее бензол использовали в качестве присадки к бензину для повышения его октанового числа, однако, сейчас, в связи с его высокой токсичностью содержание бензола в топливе строго нормируется. Иногда бензол используют в качестве растворителя. Примеры решения задачПРИМЕР 1
ПРИМЕР 2
По химическим свойствам бензол и другие ароматические углеводороды отличаются от предельных и непредельных углеводородов. Наиболее характерны для них реакции замещения атомов водорода бензольного ядра. Они протекают легче, чем у предельных углеводородов. Таким путем получают множество органических соединений. Так, при взаимодействии бензола с бромом (в присутствии катализатора FеВr 2) атом водорода замещается атомом брома: При другом катализаторе можно все атомы водорода в бензоле заместить на галоген. Это происходит, например, при пропускании в бензол хлора в присутствии хлорида алюминия: Если на бензол действовать смесью концентрированных азотной и серной кислот (нитрующей смесью), то атом водорода замещается нитрогруппой - NО 2:
Это реакция нитрования бензола. Нитробензол - бледно-желтая маслянистая жидкость с запахом горького миндаля, нерастворима в воде, применяется в качестве растворителя, а также для получения анилина. В молекуле бензола можно заместить атом водорода на алкильный радикал действием галогенопроизводных углеводородов в присутствии хлорида алюминия:
Реакции присоединения к бензолу протекают с большим трудом. Для их протекания необходимы особые условия: повышение температуры и давления, подбор катализатора, световое облучение и др. Так, в присутствии катализатора - никеля или платины - бензол гидрируется, т.е. присоединяет водород, образуя циклогексан:
Циклогексан – бесцветная летучая жидкость с запахом бензина, в воде нерастворим. При ультрафиолетовом облучении бензол присоединяет хлор:
Гексахлорциклогексан, или гексахлоран, - кристаллическое вещество, применяется как сильное средство для уничтожения насекомых. Бензол не присоединяет галогеноводороды и воду. Он очень устойчив к окислителям. В отличие от непредельных углеводородов он не обесцвечивает бромную воду и раствор KMnO 4 . В обычных условиях бензольное кольцо не разрушается и при действии многих других окислителей. Однако гомологи бензола подвергаются окислению легче предельных углеводородов. При этом окислению подвергаются лишьрадикалы, связанные с бензольным кольцом:
Таким образом, ароматические углеводороды могут вступать как в реакции замещения, так и в реакции присоединения, однако условия этих превращений значительно отличаются от аналогичных превращений предельных и непредельных углеводородов. Получение. Бензол и его гомологи в больших количествах получают из нефти и каменноугольной смолы, образующейся при сухой перегонке каменного угля (коксовании). Сухая перегонка производится на коксохимических и газовых заводах. Реакция превращения циклогексана в бензол (дегидрогенизация или дегидрирование) протекает при пропускании его над катализатором (платиновой чернью) при 300°С. Предельные углеводороды реакцией дегидрогенизации также можно превращать в ароматические. Например:
Реакции дегидрирования позволяют использовать углеводороды нефти для получения углеводородов ряда бензола. Они указывают на связь между различными группами углеводородов и на взаимное превращение их друг в друга. По способу Н.Д. Зелинского и Б.А. Казанского бензол можно получить, пропуская ацетилен через нагретую до 600° С трубку с активированным углем. Весь процесс полимеризации трех молекул ацетилена можно изобразить схемой
Реакции электрофильного замещения - реакции замещения, в которых атаку осуществляет электрофил - частица, заряженная положительно или имеющая дефицит электронов. При образовании новой связи уходящая частица - электрофуг отщепляется без своей электронной пары. Самой популярной уходящей группой является протон H + . Все электрофилы являются кислотами Льюиса. Общий вид реакций электрофильного замещения. Первая группа реакций реакции замещения. Мы говорили, что арены не имеют кратных связей в структуре молекулы, а содержат сопряженную систему из шести электронов, которая очень стабильна и придает дополнительную прочность бензольному кольцу. Поэтому в химических реакциях происходит в первую очередь замещение атомов водорода, а не разрушение бензольного кольца. С реакциями замещения мы уже сталкивались при разговоре об алканах , но для них эти реакции шли по радикальному механизму, а для аренов характерен ионный механизм реакций замещения. Первое химическое свойство галогенирование. Замещение атома водорода на атом галогена хлора или брома. Реакция идет при нагревании и обязательно с участием катализатора. В случае с хлором это может быть хлорид алюминия или хлорид железа три. Катализатор поляризует молекулу галогена, в результате чего происходит гетеролитический разрыв связи и получаются ионы. Положительно заряженный ион хлора и вступает в реакцию с бензолом. Если реакция происходит с бромом, то катализатором выступает бромид железа три или бромид алюминия.
Важно отметить, что реакция происходит с молекулярным бромом, а не с бромной водой. С бромной водой бензол не реагирует. У галогенирования гомологов бензола есть свои особенности. В молекуле толуола метильная группа облегчает замещение в кольце, реакционная способность повышается, и реакция идет в более мягких условиях, то есть уже при комнатной температуре.
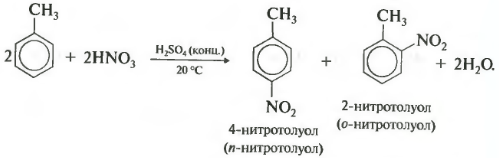
Важно отметить, что замещение всегда происходит в орто- и пара-положениях, поэтому получается смесь изомеров. Второе свойство нитрование бензола, введение нитрогруппы в бензольное кольцо.
Образуется тяжелая желтоватая жидкость с запахом горького миндаля нитробензол, поэтому реакция может быть качественной на бензол. Для нитрования используется нитрующая смесь концентрированной азотной и серной кислот. Реакция проводится при нагревании. Напомню, что для нитрования алканов в реакции Коновалова использовалась разбавленная азотная кислота без добавления серной. При нитровании толуола, также как и при галогенировании, образуется смесь орто- и пара- изомеров.
Третье свойство алкилирование бензола галогеналканами.
Эта реакция позволяет ввести углеводородный радикал в бензольное кольцо и может считаться способом получения гомологов бензола. В качестве катализатора используется хлорид алюминия, способствующий распаду молекулы галогеналкана на ионы. Также необходимо нагревание. Четвертое свойство алкилирование бензола алкенами.
Таким способом можно получить, например, кумол или же этилбензол. Катализатор хлорид алюминия. 2. Реакции присоединения к бензолуВторая группа реакций реакции присоединения. Мы говорили, что эти реакции не характерны, но они возможны при достаточно жестких условиях с разрушением пи-электронного облака и образованием шести сигма-связей. Пятое свойство в общем списке гидрирование, присоединение водорода.
Температура, давление, катализатор никель или платина. Таким же образом способен реагировать толуол. Шестое свойство хлорирование. Обратите внимание, что речь идет именно о взаимодействии с хлором, поскольку бром в эту реакцию не вступает.
Реакция протекает при жестком ультрафиолетовом облучении. Образуется гексахлорциклогексан, другое название гексахлоран, твердое вещество. Важно помнить, что для бензола не возможны реакции присоединения галогеноводородов (гидрогалогенирование) и присоединение воды (гидратация). 3. Замещение в боковой цепи гомологов бензолаТретья группа реакций касается только гомологов бензола это замещение в боковой цепи. Седьмое свойство в общем списке галогенирование по альфа-атому углерода в боковой цепи.
Реакция происходит при нагревании или облучении и всегда только по альфа-углероду. При продолжении галогенирования, второй атом галогена снова встанет в альфа-положение. 4. Окисление гомологов бензолаЧетвертая группа реакций окисление. Бензольное кольцо слишком прочное, поэтому бензол не окисляется перманганатом калия не обесцвечивает его раствор. Это очень важно помнить. Зато гомологи бензола окисляются подкисленным раствором перманганата калия при нагревании. И это восьмое химическое свойство.
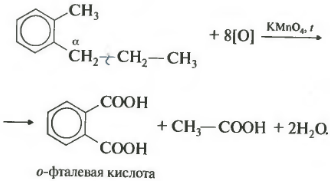
Получается бензойная кислота. Наблюдается обесцвечивание раствора. При этом, какой бы длинной не была углеродная цепь заместителя, всегда происходит ее разрыв после первого атома углерода и альфа-атом окисляется до карбоксильной группы с образованием бензойной кислоты. Оставшаяся часть молекулы окисляется до соответствующий кислоты или, если это только один атом углерода, до углекислого газа. Если гомолог бензола имеет больше одного углеводородного заместителя у ароматического кольца, то окисление происходит по тем же правилам окисляется углерод, находящийся в альфа-положении.
В данном примере получается двухосновная ароматическая кислота, которая называется фталевая кислота. Особым образом отмечу окисление кумола, изопропилбензола, кислородом воздуха в присутствии серной кислоты.
Это так называемый кумольный способ получения фенола. Как правило, сталкиваться с этой реакцией приходится в вопросах, касающихся получения фенола. Это промышленный способ. Девятое свойство горение, полное окисление кислородом. Бензол и его гомологи сгорают до углекислого газа и воды. Запишем уравнение горения бензола в общем виде. По закону сохранения массы атомов слева должно быть столько же, сколько атомов справа. Потому что ведь в химических реакциях атомы никуда не деваются, а просто изменяется порядок связей между ними. Так вот молекул углекислого газа будет столько же, сколько и атомов углерода в молекуле арена, поскольку в состав молекулы входит один атом углерода. То есть n молекул CO 2 . Молекул воды будет в два раза меньше, чем атомов водорода, то есть (2n-6)/2, а значит n-3. Атомов кислорода слева и справа одинаковое количество. Справа их 2n из углекислого газа, потому что в каждой молекуле два атома кислорода, плюс n-3 из воды, итого 3n-3. Слева атомов кислорода столько же 3n-3, а значит молекул в два раза меньше, потому как в состав молекулы входят два атома. То есть (3n-3)/2 молекул кислорода. Таким образом, мы составили уравнение сгорания гомологов бензола в общем виде. Ароматические УВ (арены) – это УВ, молекулы которых содержат одно или несколько бензольных колец. Примеры ароматических УВ:
Арены ряда бензола (моноциклические арены)Общая формула: C n H 2n-6 , n≥6 Простейшим представителем ароматических УВ является бензол, его эмпирическая формула С 6 Н 6 . Электронное строение молекулы бензолаОбщая формула моноциклических аренов C n H 2 n -6 показывает, что они являются ненасыщенными соединениями. В 1856 г. немецкий химик А.Ф. Кекуле предложил циклическую формулу бензола с сопряженными связями (чередуются простые и двойные связи) - циклогексатриен-1,3,5: Такая структура молекулы бензола не объясняла многие свойства бензола:
Проведенные позже электронографические исследования показали, что все связи между атомами углерода в молекуле бензола имеют одинаковую длину 0,140 нм (среднее значение между длиной простой связи С-С 0,154 нм и двойной связи С=С 0,134 нм). Угол между связями у каждого атома углерода равен 120 о. Молекула представляет собой правильный плоский шестиугольник. Современная теория для объяснения строения молекулы С 6 Н 6 использует представление о гибридизации орбиталей атома . Атомы углерода в бензоле находятся в состоянии sp 2 -гибридизации. Каждый атом «С» образует три σ-связи (две с атомами углерода и одну с атомом водорода). Все σ-связи находятся в одной плоскости: Каждый атом углерода имеет один р-электрон, который не участвует в гибридизации. Негибридизованные р-орбитали атомов углерода находятся в плоскости, перпендикулярной плоскости σ-связей. Каждое р-облако перекрывается с двумя соседними р-облаками, и в результате образуется единая сопряженная π-система (вспомните эффект сопряжения р-электронов в молекуле бутадиена-1,3, рассмотренный в теме «Диеновые углеводороды»): Сочетание шести σ-связей с едиой π-системой называется ароматической связью. Цикл из шести атомов углерода, связанных ароматической связью, называется бензольным кольцом, или бензольным ядром . В соответствии с современными представлениями об электронном строении бензола молекулу С 6 Н 6 изображают следующим образом:
Физические свойства бензолаБензол при обычных условиях - бесцветная жидкость; t o пл = 5,5 о С; t o кип. = 80 о С; имеет характерный запах; не смешивается с водой, хороший растворитель, сильно токсичен. Химические свойства бензолаАроматическая связь определяет химические свойства бензола и других ароматических УВ. 6π-электронная система является более устойчивой, чем обычные двухэлектроиные π-связи. Поэтому реакции присоединения менее характерны для ароматических УВ, чем для непредельных УВ. Наиболее характерными для аренов являются реакции замещения. I . Реакции замещения1.Галогенирование
2. Нитрование Реакцию осуществляют смесью и кислот (нитрующая смесь): 3.Сульфирование
4.Алкилирование (замещение атома «Н» на алкильную группу) – реакции Фриделя-Крафтса , образуются гомологи бензола:
Вместо галогеналканов можно использовать алкены (в присутствии катализатора – AlCl 3 или неорганической кислоты):
II . Реакции присоединения1.Гидрирование
2.Присоединение хлора
III. Реакции окисления1. Горение 2С 6 Н 6 + 15О 2 → 12СО 2 + 6Н 2 О 2. Неполное окисление (KMnO 4 или K 2 Cr 2 O 7 в кислой среде). Бензольное кольцо устойчиво к действию окислителей. Реакция не происходит. Получение бензолаВ промышленности: 1) переработка нефти и угля; 2) дегидрирование циклогексана:
3) дегидроциклизация (ароматизация) гексана:
В лаборатории: Сплавление солей бензойной кислоты со :
Изомерия и номенклатура гомологов бензолаЛюбой гомолог бензола имеет боковую цепь, т.е. алкильные радикалы, связанные с бензольным ядром. Первый гомолог бензола представляет собой бензольное ядро, связанное с метильным радикалом: Толуол не имеет изомеров, поскольку все положения в бензольном ядре равноценны. Для последующих гомологов бензола возможен один вид изомерии – изомерия боковой цепи, которая может быть двух видов: 1) изомерия числа и строения заместителей; 2) изомерия положения заместителей.
Физические свойства толуолаТолуол - бесцветная жидкость с характерным запахом, не растворимая в воде, хорошо растворяется в органических растворителях. Толуол менее токсичен, чем бензол. Химические свойства толуолаI . Реакции замещения1.Реакции с участием бензольного кольца Метилбензол вступает во все реакции замещения, в которых участвует бензол, и проявляет при этом более высокую реакционную способность, реакции протекают с большей скоростью. Метильный радикал, содержащийся в молекуле толуола, является заместителем рода, поэтому в результате реакций замещения в бензольном ядре получаются орто- и пара-производные толуола или при избытке реагента - трипроизводные общей формулы:
а) галогенирование
При дальнейшем хлорировании можно получить дихлорметилбензол и трихлорметилбензол:
II . Реакции присоединенияГидрирование
III. Реакции окисления1.Горение
2. Неполное окисление В отличие от бензола его гомологи окисляются некоторыми окислителями; при этом окислению подвергается боковая цепь, в случае толуола – метильная группа. Мягкие окислители типа MnO 2 окисляют его до альдегидной группы, более сильные окислители (KMnO 4) вызывают дальнейшее окисление до кислоты: Любой гомолог бензола с одной боковой цепью окисляется сильным окислителем типа KMnO4 в бензойную кислоту, т.е. происходит разрыв боковой цепи с окислением отщепившейся части ее до СО 2 ; например: При наличии нескольких боковых цепей каждая из них окисляется до карбоксильной группы и в результате образуются многоосновные кислоты, например:
Получение толуола:В промышленности: 1) переработка нефти и угля; 2) дегидрирование метилциклогексана:
3) дегидроциклизация гептана: В лаборатории: 1) алкилирование по Фриделю-Крафтсу; 2) реакция Вюрца-Фиттига (взаимодействие натрия со смесью галогенбензола и галогеналкана). |